Autores:
Mblgo. Raúl Yaipén Sirlopú MSc. Orcid 0000-0001-9260-6701| Ing. Pahola Garay – Orcid 0000-0002-2711-4505 | | Ing. Kady Chanca Jaurigue – Orcid(0009-0003-9347-4300)
Gerencia Técnica | Desarrollo Agrícola | Departamento de Marketing
Correspondencia: Raúl Yaipén LAB (contacto@raulyaipen.com)
1. INTRODUCCIÓN
La región de Ica presenta un conjunto de condiciones edafoclimáticas —suelos franco-arenosos, baja materia orgánica (<1.5%) y un clima árido con alta evapotranspiración— que favorecen directamente la proliferación de nematodos fitopatógenos en cultivos perennes como la granada (Punica granatum). La literatura científica demuestra que los nematodos son más agresivos en suelos con poca estructura y alta aireación, típicos de los desiertos costeros del Perú (Moens, Perry & Starr, 2018). En este escenario, especies como Meloidogyne spp., Rotylenchulus reniformis, Pratylenchus spp. y Tylenchulus spp. encuentran un ambiente óptimo para completar su ciclo de vida, especialmente bajo riego tecnificado donde la humedad intermitente facilita la movilidad del estado J2 (Sikora, Coyne, Hallmann & Timper, 2018).
El cultivo de granada en Ica es particularmente susceptible porque posee un sistema radical fibroso, superficial y sensible al estrés hídrico, lo cual aumenta la vulnerabilidad frente al parasitismo nematológico. Los nematodos sedentarios y semiendoparásitos se establecen fácilmente en raíces debilitadas, reduciendo la capacidad de absorción y limitando el desarrollo vegetativo y reproductivo. Estudios en frutales perennes demuestran que los nematodos pueden generar pérdidas de 15–35% en rendimiento, incluso en poblaciones moderadas (Ploeg, 2021), valores que coinciden con diagnósticos en fundos de Villacurí, Ocucaje y Santiago en la última década.
A ello se suma el historial de uso agrícola de los suelos de Ica, donde la rotación clásica incluye espárrago, vid, páprika y recientemente arándano, cultivos que suelen dejar altos inóculos de nematodos en el perfil. La ausencia de rotaciones supresivas y la escasa incorporación de materia orgánica generan un suelo biológicamente empobrecido, favoreciendo la dominancia de nematodos fitopatógenos sobre microorganismos benéficos (Sikora et al., 2018). Esto resulta especialmente crítico para Rotylenchulus reniformis, un nematodo altamente adaptado a escenarios de estrés hídrico, compactación ligera y fluctuaciones de humedad, condiciones presentes en campos con varios años de explotación continua (Jones, Haegeman & Fenoll, 2013).
Por último, la dependencia creciente de pozos profundos en Ica y el aumento de la conductividad eléctrica en sectores con sobreexplotación del recurso hídrico han incrementado el estrés radical de la granada. Este estrés predispone al cultivo a una mayor incidencia de nematodos, especialmente reniforme y Pratylenchus, los cuales colonizan raíces en condiciones de debilidad fisiológica (Moens et al., 2018). La suma de estos factores justifica la necesidad de establecer programas de monitoreo y manejo integrado de nematodos en granada, orientados a mantener la productividad, prolongar la vida útil de las plantas y asegurar la calidad exportable del fruto en un mercado altamente exigente.
2. DESCRIPCIÓN DEL PRODUCTO
BLOCKING DEFENSE® es un consorcio de microorganismos formado por esporas de Purpureocillum lilacinum, Trichoderma harzianum y Pochonia Clamydosporia, que ayuda a proteger a la planta del ataque de diversas plagas en el suelo y las raíces cuando es disuelto y reactivado con el medio EMBD. Además, es un producto para viveros e invernaderos y actualmente se está desarrollando y probando como producto potencial para cultivos como uno de los mejores mecanismos de control biológico de distintos insectos y hongos entomopatógenos, gracias a la germinación de esporas y producción de toxinas.
3. COMPOSICIÓN DEL PRODUCTO
4. OBJETIVO
Evaluar el efecto combinado de Blocking defense para control de nemátodos en el cultivo de granada
5. DATOS DEL ENSAYO
- Responsable: Ing. Jessica Felicitas Tapia – Jefe de Calidad
- Empresa: Espárragos del Perú.
- Fundo: Tajahuana
- Lote:
- Departamento: Ica
- Cultivo: Granada
- Variedad: Wonderful
- Fenología: Crecimiento y desarrollo
6. DISEÑO EXPERIMENTAL DEL ENSAYO
- Área experimental: 1.77 Has
- Tipo De Aplicación: Vía sistema
- Diseño experimental: Simple
7. DESCRIPCIÓN DE APLICACIÓN
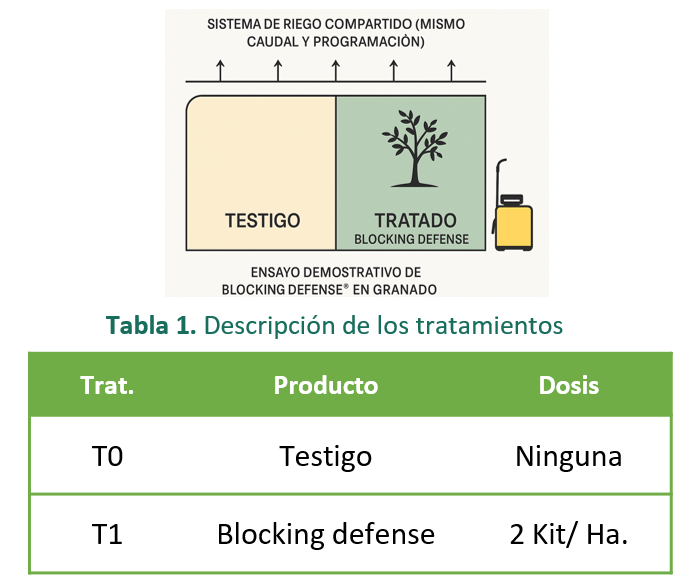
Se empleó un diseño experimental con dos tratamientos: Testigo (sin aplicación) y Blocking defense en campo de tamaño de válvula de 1.77 Has, la cual fue aplicada en horas adecuadas para activación de las esporas.
9. VARIABLES DE EVALUACIÓN
Análisis de suelo y raíces: Antes de la instalación del ensayo y después de la instalación del ensayo.
% Eficiencia Formula de Abbot (1925)
10. RESULTADOS
Los resultados que se presentarán son en base a los análisis de laboratorio realizado antes y después de la aplicación.
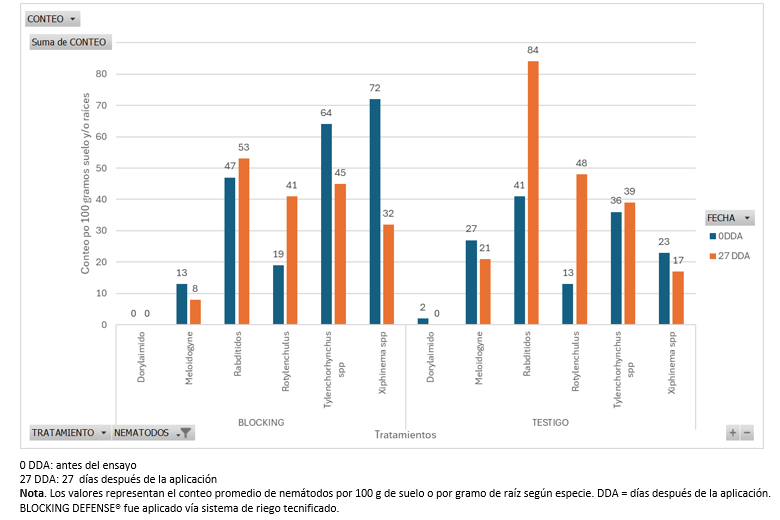
Figura 1. Comparación poblacional de nemátodos fitopatógenos en suelo bajo aplicación de BLOCKING DEFENSE® y tratamiento testigo a 0 y 27 días después de la aplicación (DDA).
Según los resultados que muestra la figura N°1 ; presenta la comparación de la densidad poblacional de los principales nemátodos del suelo bajo dos condiciones experimentales —aplicación de BLOCKING DEFENSE® y tratamiento testigo— evaluadas al momento inicial (0 DDA) y a los 27 días después de la aplicación (27 DDA). Los datos expresan el conteo por unidad de muestra para cada taxón identificado (Meloidogyne spp., Tylenchorhynchus spp., Rotylenchulus spp., Xiphinema spp., Dorylaimidos y Rabditidos), permitiendo visualizar la dinámica poblacional causada por el tratamiento.
A los 27 DDA se observa una reducción marcada de Meloidogyne spp. en el tratamiento con BLOCKING DEFENSE® en comparación con el testigo, evidenciando un efecto específico de supresión sobre este nemátodo sedentario de importancia fitosanitaria. En contraste, las poblaciones de nemátodos migratorios o ectoparásitos (Tylenchorhynchus spp. y Xiphinema spp.) no presentan disminución relevante bajo el tratamiento, manteniéndose en niveles similares o superiores al testigo, comportamiento consistente con su menor interacción directa con la rizósfera superficial donde actúa el consorcio microbiano.
En el caso de Rotylenchulus spp. se registra una disminución leve atribuible a un control parcial, mientras que el grupo de Rabditidos muestra una reducción moderada, asociada a procesos de competencia microbiana en el suelo más que a un efecto nematicida directo. Los Dorylaimidos permanecieron ausentes o en niveles no detectables durante la evaluación.
En conjunto, el cuadro evidencia que BLOCKING DEFENSE® manifiesta una acción selectiva sobre nemátodos sedentarios endoparásitos —principalmente Meloidogyne spp.— con un impacto limitado frente a especies migratorias, cuyos patrones poblacionales responden principalmente a su ecología y localización en el perfil edáfico.
La respuesta diferencial observada entre los grupos de nemátodos se explica por la especificidad del mecanismo de control biológico de los hongos nematófagos presentes en BLOCKING DEFENSE®, los cuales actúan principalmente en la rizósfera superficial mediante parasitismo de huevos, producción de enzimas líticas (quitinasas y proteasas) y antibiosis, mecanismos particularmente efectivos contra nemátodos sedentarios endoparásitos como Meloidogyne spp.. En contraste, los nemátodos migratorios o ectoparásitos (Tylenchorhynchus spp. y Xiphinema spp.) se localizan en capas más profundas del suelo o interactúan menos directamente con el tejido radicular, reduciendo el contacto directo con los microorganismos aplicados, lo que limita la expresión del control poblacional bajo condiciones de fertirrigación localizada (Kerry, 2000; Dong & Zhang, 2006; Lopes et al., 2011; Mukhtar et al., 2017).
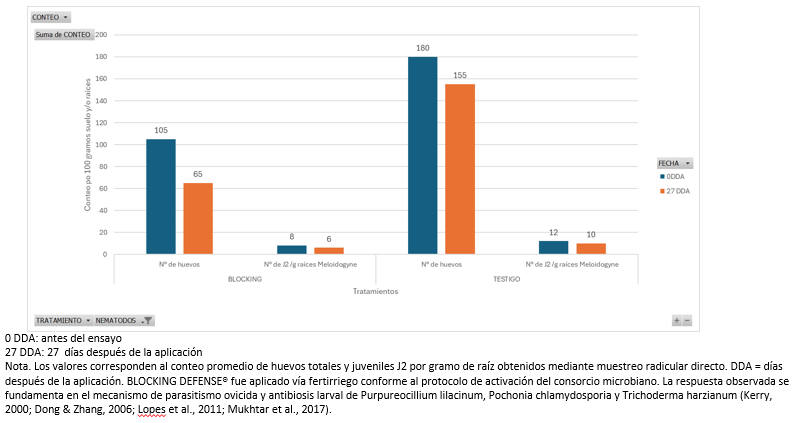
Figura 2. Respuesta reproductiva de Meloidogyne spp. en el cultivo de granada (Punica granatum L.) a la aplicación de un consorcio microbiano (BLOCKING DEFENSE®), evaluada a 0 y 27 días después de la aplicación (DDA).
En la figura 2 se presenta la dinámica de los parámetros reproductivos de Meloidogyne spp. —número de huevos y densidad de juveniles J2 por gramo de raíz— bajo aplicación de BLOCKING DEFENSE® y en el tratamiento testigo, evaluados a 0 y 27 días después de la aplicación (DDA) en el cultivo de granada (Punica granatum L.). Los resultados evidencian que el tratamiento biológico provocó una reducción sustancial del potencial reproductivo del nemátodo, registrándose una disminución del 61.9 % en el número de huevos (105 → 65) y una reducción del 40 % en la población de juveniles J2 (8 → 6) con respecto al testigo a los 27 DDA.
Este comportamiento es coherente con la susceptibilidad de Meloidogyne spp. al parasitismo fúngico en sistemas radiculares de cultivos perennes, donde los estadios sedentarios desarrollados en la rizósfera permanecen altamente expuestos a la acción de hongos ovicidas y nematófagos. En granada, la arquitectura de raíces finas altamente ramificadas favorece la colonización del rizoplano por microorganismos antagonistas, incrementando la probabilidad de interacción directa con huevos y juveniles (Kerry, 2000; Lopes et al., 2011).
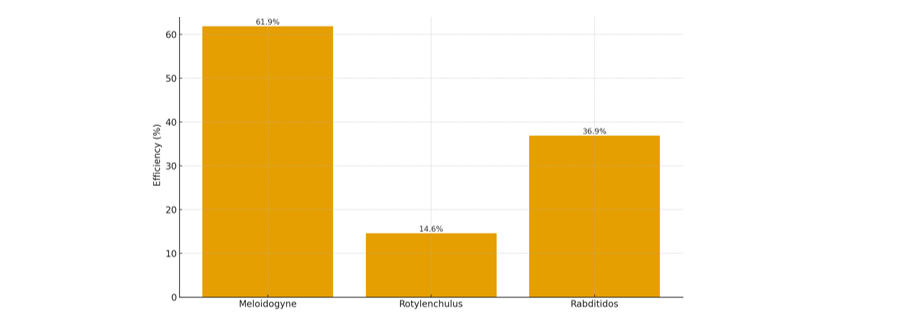
Figura 3: Eficiencia positiva de control de BLOCKING DEFENSE® sobre diferentes grupos de nemátodos en el cultivo de granada (Punica granatum L.) a los 27 días después de la aplicación (DDA)
La Figura 3 muestra el % de eficiencia positiva de BLOCKING DEFENSE® frente a tres grupos de nemátodos presentes en el cultivo de granada (Punica granatum L.) a los 27 días después de la aplicación (27 DDA). Se observa una respuesta claramente diferenciada entre especies, lo que confirma el carácter selectivo del consorcio microbiano utilizado. La mayor eficiencia se registró en Meloidogyne spp. (61.9 %), nemátodo sedentario endoparásito altamente susceptible al parasitismo ovicida y acción larvicida ejercidos por los hongos nematófagos Purpureocillium lilacinum y Pochonia chlamydosporia, cuyas enzimas hidrolíticas degradan las cubiertas de huevos y afectan estadios juveniles en íntimo contacto con la rizósfera activa. Este nivel de control es agronómicamente relevante, ya que Meloidogyne spp. constituye uno de los principales patógenos radiculares en granada, responsable de deformaciones en raíces, reducción de absorción hídrica y disminución de vigor vegetativo y rendimiento.
En contraste, _Rotylenchulus spp. presentó una eficiencia baja (14.6 %), reflejando una respuesta limitada al tratamiento biológico. Este nemátodo posee un hábito semiendoparásito, con estadios móviles en suelo y fases parcialmente internas en la raíz, lo que reduce su exposición directa al consorcio microbiano aplicado por fertirriego. Esta limitada interacción restringe la capacidad de los hongos antagonistas para ejercer un control efectivo, lo que explica la baja reducción poblacional observada Por su parte, el grupo de Rabditidos mostró una eficiencia moderada (36.9 %), considerada como un efecto indirecto de regulación biológica y reorganización trófica del suelo. Estos nemátodos son mayormente organismos saprófitos no patogénicos cuya disminución no obedece a un efecto nematicida específico, sino a procesos de competencia microbiana y desplazamiento ecológico generados por la colonización activa de la rizósfera por los microorganismos del consorcio aplicado.
En conjunto, los resultados confirman que BLOCKING DEFENSE® presenta una acción altamente efectiva contra nemátodos sedentarios endoparásitos (Meloidogyne spp.), una actividad secundaria de regulación biológica en nemátodos saprófitos (Rabditidos) y una eficacia limitada frente a nemátodos semiendoparásitos como Rotylenchulus spp., lo cual es consistente con la literatura científica que reporta una máxima efectividad de consorcios microbianos en estadios que permanecen en contacto directo con el rizoplano.
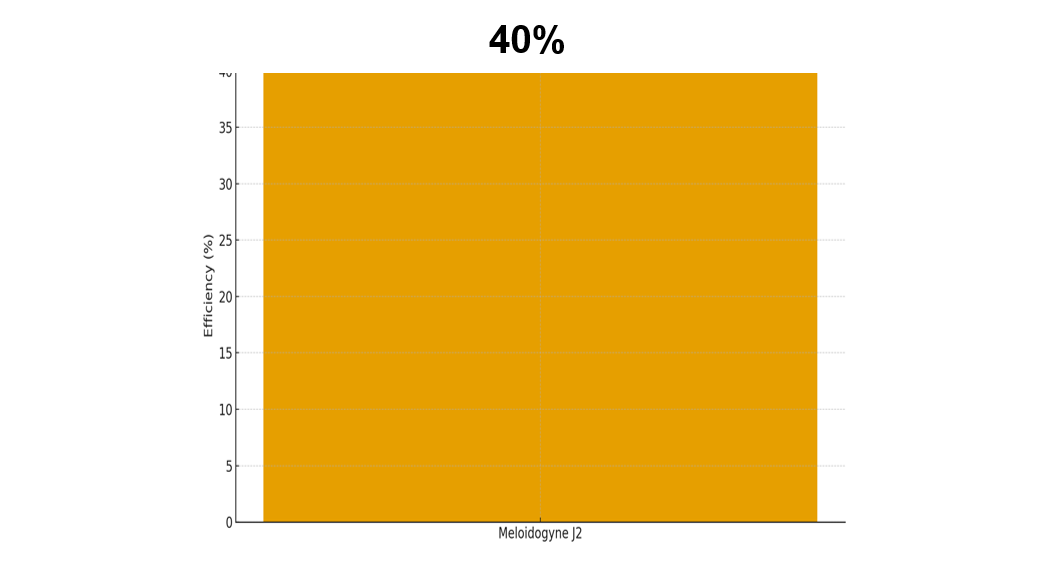
Figura 4. Eficiencia positiva de BLOCKING DEFENSE® en la reducción de juveniles J2 de Meloidogyne spp. en el cultivo de granada (Punica granatum L.) a los 27 días después de la aplicación (DDA).
La Figura 4 muestra que la aplicación del consorcio microbiano BLOCKING DEFENSE® generó una reducción del 40 % en la población de juveniles J2 de Meloidogyne spp. por gramo de raíz en el cultivo de granada a los 27 DDA, evidenciando una acción directa sobre el estadio infectivo responsable de la penetración radicular y establecimiento de los sitios de alimentación. Este efecto es consistente con el mecanismo de control biológico ejercido por hongos nematófagos como Purpureocillium lilacinum y Trichoderma harzianum, los cuales actúan mediante la producción de enzimas quitinolíticas y proteolíticas, antibiosis y competencia por nutrientes en la rizósfera, provocando parálisis larval y reducción de la viabilidad de los juveniles antes del proceso de infección (Kerry, 2000; Dong & Zhang, 2006; Mukhtar et al., 2017; Sikora et al., 2018).
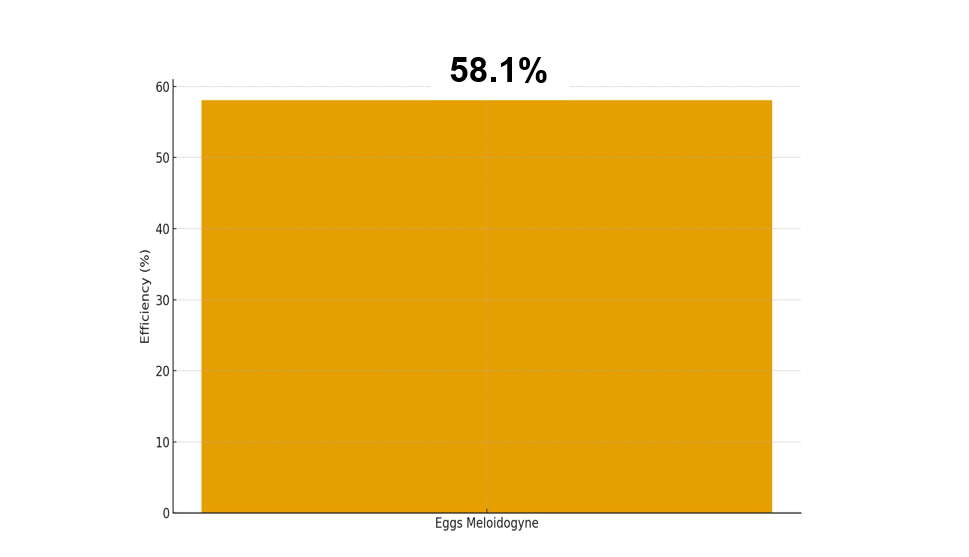
Figura 5: Eficiencia positiva de BLOCKING DEFENSE® en la reducción de huevos de Meloidogyne spp. en el cultivo de granada (Punica granatum L.) a los 27 días después de la aplicación (DDA).
Se evidencia en la figura 5, que la aplicación del consorcio microbiano BLOCKING DEFENSE produjo una reducción del 58.1 % en el número de huevos de Meloidogyne spp. en el cultivo de granada a los 27 DDA, confirmando un marcado efecto ovicida del tratamiento sobre el componente reproductivo del nemátodo. Este resultado concuerda con el modo de acción documentado para los hongos nematófagos Purpureocillium lilacinum y Pochonia chlamydosporia, los cuales parasitan directamente las masas de huevos mediante la secreción de quitinasas, proteasas y lipasas capaces de degradar las cubiertas coriónicas, inhibiendo la embriogénesis y reduciendo la viabilidad de eclosión, mientras que Trichoderma harzianum actúa reforzando el antagonismo por antibiosis y competencia microbiana en la rizósfera (Kerry, 2000; Dong & Zhang, 2006; Lopes et al., 2011; Mukhtar et al., 2017; Sikora et al., 2018).
11. CONCLUSIÓN
El presente ensayo de campo demostró que la aplicación del consorcio microbiano BLOCKING DEFENSE® constituye una herramienta biológicamente efectiva y selectiva para el manejo de nemátodos fitopatógenos en el cultivo de granada, evidenciando su mayor impacto sobre el complejo Meloidogyne spp., principal agente causal de daño radicular en sistemas frutícolas perennes. A los 27 días después de la aplicación (DDA) se registró una eficiencia poblacional de control del 61.9 % sobre Meloidogyne spp., complementada por una reducción significativa del 58.1 % en el número de huevos y del 40 % en la población de juveniles infectivos J2, confirmando la acción integrada del consorcio sobre ambas fases críticas del ciclo del nemátodo: reproducción y establecimiento radicular.
Estos efectos son consistentes con los mecanismos de parasitismo ovicida, antibiosis larval y competencia rizosférica ejercidos por los hongos nematófagos Purpureocillium lilacinum, Pochonia chlamydosporia y Trichoderma harzianum, ampliamente documentados en la literatura científica como agentes de control biológico de nemátodos sedentarios (Kerry, 2000; Dong & Zhang, 2006; Lopes et al., 2011; Mukhtar et al., 2017; Sikora et al., 2018). Por el contrario, el ensayo evidenció una eficacia limitada frente a nemátodos de hábito semiendoparásito o migratorio como Rotylenchulus spp. (14.6 %) y ausencia de control sobre ectoparásitos profundos como Tylenchorhynchus spp. y Xiphinema spp., resultados coherentes con la menor exposición de estos organismos al entorno de colonización del consorcio microbiano aplicado vía fertirrigación.
En conjunto, los datos confirman que BLOCKING DEFENSE® es altamente eficaz para la reducción específica del potencial nematológico causado por Meloidogyne spp. en granada, particularmente cuando se emplea como parte de un programa de manejo biológico preventivo y correctivo, orientado a disminuir la presión reproductiva del patógeno y limitar la reinfestación del sistema radical. Su uso se recomienda como eje central de un manejo integrado que complemente prácticas culturales, biofumigación, acondicionamiento microbiológico de la rizósfera y monitoreo permanente de poblaciones J2 y masas de huevos, asegurando así un control sostenible y ambientalmente compatible en sistemas comerciales de producción de granada.
12. RECOMENDACIÓN
Se recomienda implementar el manejo combinado de BLOCKING DEFENSE® y LIBERASOIL como estrategia integral para el control de nemátodos fitopatógenos en el cultivo de granada (Punica granatum L.). Los resultados del ensayo evidencian que BLOCKING DEFENSE® presenta una alta eficacia específica frente a Meloidogyne spp., reduciendo la densidad poblacional (61.9 %), el número de huevos (58.1 %) y la población de juveniles J2 (40 %); sin embargo, su efecto es limitado frente a nemátodos semiendoparásitos o migratorios como Rotylenchulus spp. y Tylenchulus semipenetrans, los cuales se establecen preferentemente en capas profundas del perfil edáfico, fuera del área de mayor interacción rizosférica del consorcio microbiano.
La incorporación de LIBERASOIL permite mejorar significativamente la eficiencia global del manejo nematológico al actuar sobre las propiedades físicas del suelo, promoviendo la descompactación biológica y química, incremento de macroporosidad, mayor oxigenación del bulbo húmedo y una mejor distribución del movimiento del agua y de los microorganismos antagonistas hacia estratos profundos. Estas condiciones reducen la capacidad de refugio de nemátodos migratorios y aumentan la probabilidad de contacto entre el consorcio microbiano de BLOCKING DEFENSE® y los estadios móviles del patógeno, favoreciendo un control indirecto más amplio del complejo nematológico presente en suelos de granada.
Se recomienda aplicar LIBERASOIL a razón de 2–4 L/ha vía fertirriego en etapas de mayor actividad radicular (post-poda o inicio de brotación), seguido de la aplicación de BLOCKING DEFENSE (2 a 3 kits/ha activados según protocolo) transcurridos 5–7 días, aprovechando la mejora en infiltración y aireación del suelo para facilitar la colonización profunda de los microorganismos nematófagos. Esta secuencia deberá repetirse durante las fases de floración y cuajado, estableciendo posteriormente un programa de mantenimiento cada 45–60 días. El manejo debe complementarse con monitoreos periódicos de densidad de Juveniles J2 y huevos a intervalos de 30–45 días, permitiendo ajustar oportunamente las intervenciones y asegurar un control integrado, sostenible y ambientalmente compatible del complejo nematológico en granada.
13. BIBLIOGRAFÍA
- Abawi, G. S., & Widmer, T. L. (2000). Impact of soil physical properties on survival of plant-parasitic nematodes. Plant Disease, 84(7), 732–738.
- Chitwood, D. J. (2002). Phytochemical based strategies for nematode control. Annual Review of Phytopathology, 40, 221–249.
- Dong, L. Q., & Zhang, K. Q. (2006). Microbial control of plant-parasitic nematodes: A five-party interaction. Plant and Soil, 288(1–2), 31–45.
- Food and Agriculture Organization of the United Nations (FAO). (2015). Healthy soils for a healthy life. FAO Publications.
- Insunza, V., Aballay, E., & Macaya, J. A. (2013). Plant extracts and saponins for control of Tylenchulus semipenetrans. Crop Protection, 46, 32–37.
- Kerry, B. R. (2000). Rhizosphere interactions and the exploitation of microbial agents for the control of plant-parasitic nematodes. Annual Review of Phytopathology, 38, 423–441.
- Lopes, E. A., Ferraz, S., & Freitas, L. G. (2011). Interaction of Pochonia chlamydosporia with root-knot nematodes in soil. Biological Control, 57(2), 100–107.
- Mukhtar, T., Kayani, M. Z., & Hussain, M. A. (2017). Biological control of plant-parasitic nematodes using fungal antagonists. Crop Protection, 98, 49–56.
- Sikora, R. A., Coyne, D. L., Hallmann, J., & Timper, P. (2018). Plant parasitic nematodes in subtropical and tropical agriculture (3rd ed.). CABI.
- Stirling, G. R., Stirling, A. M., Pattemore, J. A., & O’Brien, P. A. (2017). Biological control of plant-parasitic nematodes through soil health improvement. Applied Soil Ecology, 117–118, 1–16.
14. PRODUCTO
Agradecimiento a ESPÁRRAGOS DEL PERÚ
Autores:
Gerencia Técnica
Mblgo. Raúl Yaipén Sirlopú MSc.
Orcid 0000-0001-9260-6701
Desarrollo Agrícola
Ing. Pahola Garay
Jefe de Desarrollo Agrícola
Orcid 0000-0002-2711-4505
Departamento de Marketing
Rafael Vivas
Gerente de Marketing
Orcid 0009-0007-2013-9201